|
尚廷A8新版GMP质量管控系统
“尚廷A8新版GMP质量管控系统”包括11个子系统,分别是:机构与人员,厂房与设施,设备管理,物料与产品,确认与验证,文件管理,生产管理,质量控制与质量保证,委托生产与委托检验,产品发运与召回,自检。
“尚廷A8新版GMP质量管控系统”的架构设计完全符合计算机验证的要求,可进行审查追踪,并实现电子记录与电子签名以符合PDA 21 CFR Part 11的要求。
一、“尚廷A8新版GMP质量管控系统”的价值
1.1尚廷A8新版GMP质量管控系统是以2010新版GMP规范为基础,专注制药行业,形成对药品质量“动态,全生命周期的过程管理”!形成以质量保证系统(QA)和质量控制系统(QC) 及GMP文件管理、培训管理为核心,将影响质量的各部门:生产部门,工艺部,采购部,物料中心,质量管理部门、实验室、销售部门、设备部门、中高层领导都纳入到统一的质量监管平台中,是新版GMP在企业落地的最佳工具,真正实现GMP的长效管理。
1.2已通过新版GMP及CGMP认证的制药企业,可将企业GMP体系,规范,制度,SOP,文件等固化到“尚廷A8新版GMP质量管控系统”中,减少人为差错,增强日常操作合规性。
1.3领导需要的各种质量管控报表,“尚廷A8新版GMP质量管控系统”可一键查询和打印,省却人工统计的等待时间,增强统计结果的准确性和及时性。
1.4质量部门从日常重复,繁琐的劳动中解放出来,“尚廷A8新版GMP质量管控系统”可使质量部在不增加本部门工作人员或减少一定人员的情况下完成日益繁重的GMP认证工作及日常工作,真正实现“优化质量管控流程,向管理要效益的目标”。
二、下面就其中几个子系统做专门介绍:
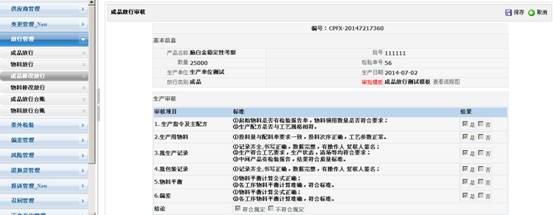
2.1 质量保证系统:
变更管理,验证管理,退换货管理,召回管理,投诉管理,稳定性管理,放行管理,偏差管理,内审管理,不合格品管理,CAPA,年度质量回顾,标准管理,供应商管理,审计追踪,委外检验。

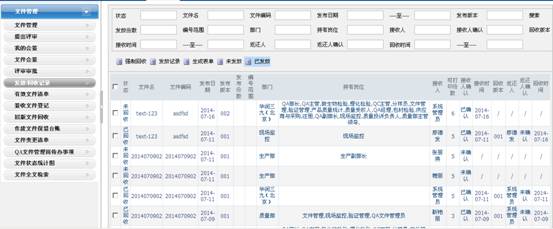
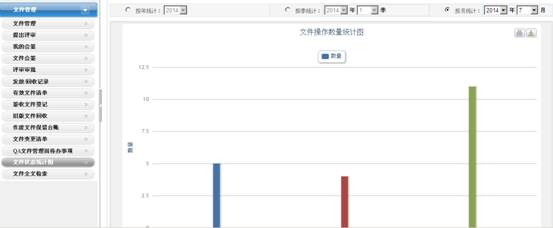
2.2 GMP文件管理系统:
尚廷A8 GMP文件管理系统是依据 GMP 法规中对GMP 文件的管理规程,融合尚廷团队丰富的文件管理流程实务经验,所研发的电子化 GMP 文件管理系统。尚廷A8 GMP文件管理系统能管理完整的 GMP 文件生命周期,从文件创建,模板选择,文件审核流程,文件批准,文件分发,文件启用,到版本管理,版本差异对照,关键字查询,文件变更(文件修订,文件作废,文件到期评审,重大变化关联评审等),对所有 GMP 文件进行合规高效的管理。系统应用后,企业的文件管理事半功倍,大幅提高工作效率,能更轻松的通过药监局的检查。
尚廷A8 GMP文件管理系统的架构设计完全符合计算机验证的要求,可进行审查追踪,并实现电子记录与电子签名以符合FDA 21 CFR Part 11 的要求。
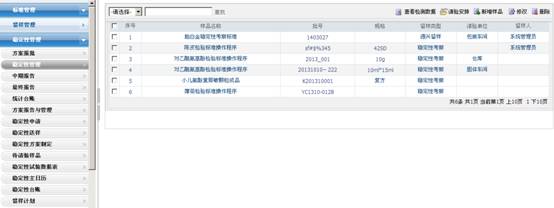
2.3 实验室管理系统(LIMS):
尚廷A8实验室管理系统能够电子化的支持取样管理,检验管理,稳定性考察,OOS超标调查管理,仪器设备管理,环境监测,水系统管理,实验耗材管理等流程,实现即时报表与分析工作,并与主要仪器设备完成接口,直接导入检验数据,减少人为录入的失误,为实验室管理水平的整体提高和实验室的全面管理提供先进的技术支持。
检验管理:
取样管理,样品登记,自动编号,标签打印,单据模板打印,智能录入方式,检测项目分配,任务分配,结果录入,多级数据审核,记录和报告,放行管理。
实验室管理:
OOS超标调查管理,留样管理,稳定性管理,环境监测,计量管理,仪器管理,成本管理,水系统管理,实验耗材管理。
|