1. 行业背景
为贯彻落实《国务院关于加强食品等产品安全监督管理的特别规定》和《国务院办公厅关于进一步加强药品安全监管工作的通知》(国办发〔2007〕18号),加快建立重点药品安全追溯体系,强化药品质量安全监管,确保公众用药安全,国家局决定,在特殊药品监控信息网络基础上,进一步加强药品电子监管,完善药品标识制度,建立全国统一的药品电子监督管理网络(以下简称药品电子监管网),分类分批对药品实施电子监管。
2007年10月1日,我国特殊药品监控系统正式开通,实现了对麻醉药品和第一类精神药品的实时监控。
2008年首批《入网药品目录》为血液制品、疫苗、中药注射剂及第二类精神药品等。即2008年10月31日前完成赋码入网,要在全国范围内基本实现对血液制品、疫苗、中药注射剂及第二类精神药品等重点药品的生产、经营情况实行实时监控;将目录中已批准注册的药品生产、经营企业纳入实时监控,这些重点药品在上市前必须在产品最小销售包装上加贴统一标识的药品监管码。未使用药品电子监管码统一标识的,一律不得销售。
2010-4-20日,《国务院办公厅关于印发医药卫生体制五项重点改革2010年度主要工作安排的通知》中明确提出:全面提高和完善307种国家基本药物的质量标准,对基本药物进行全品种覆盖抽验和全品种电子监管,至此,纳入医保报销范围比例最大的基本药物将全部实现电子监管。
为此尚廷科技开发出了《尚廷A8药品赋码系统》,该系统是完整的电子赋码系统,因此各大企业通过赋码系统,包装赋码后,可以实现从原材料投入,到生产环节,直至最终的出入库等流通环节,实现了整个企业的供应链管理,快速有效的对有问题的产品进行追溯和召回,尽可能的减少企业的损失。
2. 系统目标

3. 业务价值

1) 通过药品赋码系统,可以满足监管部门和企业对产品监管码数据的要求。
2) 通过药品赋码系统,可以增加对质量问题产品进行精确监控、追溯,对有可能出现的药品安全隐患进行有效评估和科学预警依据,避免企业经营的损失,提升产品在市场的形象,维护企业形象和商品声誉。
3) 通过药品赋码系统,可以实现产品追溯过程,相比记录档案追溯方式更加高效,实时,便捷,大大提高企业的效率,提升企业的利润。
4. 系统结构图
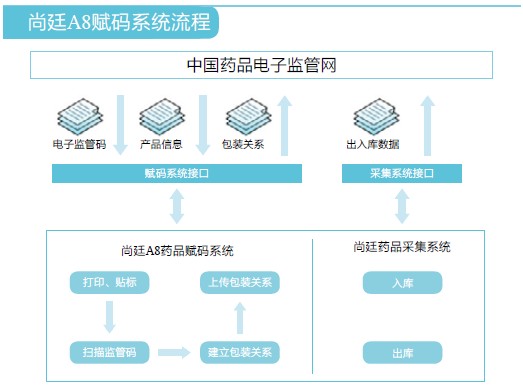
5. 系统赋码原理
1) 对生产包装过程的产品小盒、中盒、大箱,进行唯一身份码的赋码,并将多级包装的身份码进行父子关系的关联,把关联关系储存在数据库中,将监管码关联数据通过数据接口发送到特殊食品药品监控信息网络系统,这些关系将是国家监管和企业实现防伪防窜货的重要数据来源
2) 从生产赋码,到一级扫描,建立一级关系,再到二级包装,建立二级关系,到三级扫描建立三级关系,到最终的入库的整个环节。
3) 尚廷A8 通三级条码关系加以关联,建立各级包装包装关联关系。

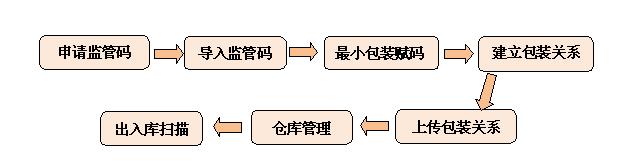
6. 方案简介
1) 申请监管码:在监管网平台上申请监管码。
2) 导入监管码:首先在监管网平台上解密监管码,然后再在生产线赋码系统中,通过监管码导入功能。
3) 最小包装赋码:将监管码在企业实际生产包装前或包装后附着在产品的最小包装上。
4) 建立包装关系:在产品包装的过程中,通过条码数据采集设备,对每级包装内的监管码进行数据采集,并根据包装比例,完成相应的产品与外包装的监管码包装关系,具体的生产线的包装赋码方式见详细赋码方案;
5) 上传关联关系:生产结束后,需要将生产过程中形成的监管码的包装关系上传到监管网平台。
6) 出入库扫描:在监管网平台中称为“核注核销”,主要是将企业的入库的监管码的数据信息与出库的监管码的数据信息全部进行记录,能够详细的跟踪到药品的出入库流向,此部分功能主要是通过手持数据采集终端进行处理。
7.系统效益

|